FAQ
Veelgestelde vragen n.a.v. de publicatie in eClinicalMedicine
Toen wij de eerste Long COVID patiënten in onze pijnkliniek zagen, was dat in eerste instantie in het kader van behandeling van ernstige neuropathische pijn. Deze patiënten hadden langdurige klachten na Covid-19 en er waren nauwelijks effectieve behandelopties. We behandelden hen daarom met intraveneuze lidocaïne, zoals gebruikelijk is bij therapieresistente neuropathische pijn. Wat ons opviel, was dat niet alleen de pijn, maar ook andere Long COVID-klachten begonnen af te nemen: klachten als brain fog, post-exertional malaise, overprikkeling en autonome klachten namen eveneens duidelijk af.
Dat patroon, verbetering van pijn én neurologisch/cognitieve klachten onder één behandeling, paste bij de hypothese dat Long COVID in belangrijke mate een (neuro-)inflammatoire aandoening is, waarbij ontstekingsprocessen in zenuwstelsel en immuunsysteem een centrale rol spelen. Lidocaïne is immers niet alleen een lokaal verdovend middel, maar heeft ook systemische anti-inflammatoire eigenschappen, met name op neuroinflammatie. Vanuit dat klinische beeld is het idee ontstaan om lidocaïne langduriger en gerichter in te zetten.
Intraveneuze toediening vraagt echter om ziekenhuisopname en continue monitoring van vitale functies, en is daardoor niet geschikt als thuisbehandeling. Daarom is gekozen voor ontwikkeling van een subcutane formulering van lidocaïne met hydroxypropyl-β-cyclodextrine (HP-β-CD), bedoeld om langer in het lymfestelsel aanwezig te blijven, lagere plasmaspiegels te geven en zo de kans op toxiciteit te verkleinen.
De patiënten die in het artikel worden beschreven, zijn geen vooraf gerandomiseerde onderzoekspopulatie, maar ernstig zieke mensen die door hun huisarts naar ons werden verwezen voor (pijn) behandeling. Gezien de ernst en duur van hun klachten vonden wij het ethisch moeilijk verdedigbaar om deze groep eerst nog jaren in een klassieke placebogecontroleerde trial te plaatsen. In de praktijk betekent dat minstens één tot twee jaar voordat een eerste patiënt behandeld mag worden. In die periode zouden deze patiënten dan géén toegang hebben tot een behandeling waarvan we al zagen dat zij er klinisch duidelijk op vooruit gingen.
In plaats daarvan hebben we gekozen voor een zorgtraject met zeer intensieve monitoring, waarbij we vanaf het moment van intake systematisch data verzamelden. Patiënten kregen een wearable (Oura-ring) die onder andere hartslag, activiteit en slaap registreerde, en een app waarin zij dagelijks de ernst van hun klachten doorgaven en tweewekelijks vragenlijsten invulden. Omdat de productie van de lidocaïne-HP-β-CD-formule via een ziekenhuisapotheek moest worden opgestart, ontstond er een observatieperiode van gemiddeld vier weken vóór de eerste injectie. In die periode kregen patiënten nog geen medicatie, maar werden al wel gemonitord.
Daarmee werd iedere patiënt zijn eigen controle: we konden het beloop tijdens de pre-behandelingsfase vergelijken met het beloop tijdens de behandelingsfase. Achteraf zijn deze data, met terugwerkende kracht, samen met onderzoekers van de VU en het Amsterdam UMC geanalyseerd in een Interrupted Time Series-opzet. Dat is een observationeel design dat, mits goed uitgevoerd en in een populatie met chronisch zieke patiënten zoals deze, de statistische zeggingskracht van een RCT kan benaderen, zonder dat ernstig zieke mensen jarenlang een potentieel werkzame behandeling wordt onthouden.
Het is belangrijk om te benadrukken dat dit het eerste wetenschappelijke artikel over deze behandeling is, dat vanzelfsprekend niet alle vragen al beantwoordt. De resultaten laten zien dat een aanzienlijk deel van de patiënten met ernstige Long Covid klachten duidelijke verbetering ervaart in kwaliteit van leven en symptoomlast. Die effecten variëren van bescheiden, maar voor de patiënt goed merkbare vooruitgang, tot vrijwel volledig verdwijnen van klachten. Met goede prikinstructies kunnen patiënten de subcutane injecties bovendien zelf thuis toedienen.
Tegelijk gaat het om een observationele studie, zonder gerandomiseerde placebo groep, uitgevoerd in een gespecialiseerde klinische setting. Methodologisch is gebruikgemaakt van een interrupted time series-design met intensieve metingen vóór en tijdens de behandeling. Dit ontwerp benadert, volgens prof dr J.W.R. Twisk (hoogleraar statistiek en methodologie AUMC), mits goed uitgevoerd in een stabiele chronische populatie zoals deze, de statistische zeggingskracht van een gerandomiseerde trial, maar het blijft formeel een observationele studie. Dat betekent dat de bevindingen veelbelovend zijn, maar nog bevestigd moeten worden in een RCT. Voor formele registratie van de behandeling wordt gewerkt aan de opzet van zo’n RCT, waarin een deel van de patiënten de actieve behandeling krijgt en een deel placebo. Een dergelijk onderzoek kan al snel 2 jaar duren. Daarnaast zijn er ook ethische en praktische bezwaren om placebo te geven bij ernstig zieke patiënten.
Wij vinden op basis van de huidige gegevens dat de therapie voldoende onderbouwd is om door te gaan met behandelen, met name in gespecialiseerde centra met ervaring en digitale monitoring. In combinatie met de grote, onbeantwoorde zorgvraag bij ernstig zieke long-covid patiënten achten wij het niet verantwoord om vanwege de zeer dringende hulpvraag van de duizenden long COVID patiënten deze behandeling nu “on hold” te zetten in afwachting van nóg meer bewijs.
Dat betekent niet dat aanvullend onderzoek niet nodig blijft, integendeel: gerandomiseerde studies, langere termijn opvolging en beter inzicht in welke patiënten het meest profiteren zijn essentieel voor verdere verfijning en eventuele formele registratie en pakketbeoordeling. Maar wij zien de huidige resultaten als voldoende sterk om de behandeling nú beschikbaar te houden voor patiënten bij wie andere opties ontbreken, parallel aan het opzetten van vervolgonderzoek.
Het klopt dat generiek Lidocaïne als grondstof goedkoop is. De behandeling waarover wij publiceren betreft echter niet het standaard Lidocaïne, maar een speciaal ontwikkelde formulering voor dagelijkse thuistoediening en gerichte opname via het lymfatische systeem en de lymfeklieren.
Voor deze toepassing is Lidocaïne:
- Farmaceutisch aangepast om na subcutane toediening preferentieel via het lymfesysteem te worden opgenomen in plaats van via de bloedbaan.
- Geformuleerd met specifieke hulpstoffen, in een nauwkeurig gecontroleerde samenstelling, zodat effectieve immuunmodulatie mogelijk is bij lage en veilige plasmaconcentraties.
- Geschikt voor veilige zelftoediening thuis, waardoor belastende en kostbare ziekenhuisbehandelingen worden voorkomen.
De medicatie:
- Wordt tot op heden op relatief kleine schaal bereid door een ziekenhuisapotheek,
- Dit geschiedt volgens strikte kwaliteits- en veiligheidsnormen (GMP/GDS),
- Kent hoge bijbehorende kosten voor farmaceutische validatie, kwaliteitscontrole, verpakking, distributie en medische monitoring (deels digitaal).
Juist deze kleinschalige, bereiding door een ziekenhuisapotheek verklaart een belangrijk deel van de huidige kosten.
Tegelijkertijd worden voorbereidingen getroffen om de productie in samenwerking met een internationale grootbereider op korte termijn op te schalen. Door deze opschaling:
- Kunnen productieprocessen worden gestandaardiseerd,
- Neemt de efficiëntie sterk toe, en
- Daardoor zal de kostprijs per patiënt naar verwachting fors dalen.
Samenvattend:
Het gaat niet om “dure lidocaïne”, maar om een formulering geschikt voor dagelijkse thuistoediening die momenteel kleinschalig wordt bereid en die bij internationale opschaling aanzienlijk goedkoper kan worden.
Nee. Dit betreft een doorgeleverd (magistraal) bereid middel: een gebruikelijke werkwijze waarbij, in samenwerking tussen behandelend arts en apotheker, een bestaande geregistreerde werkzame stof (lidocaïne) met een hulpstof wordt bereid voor een specifieke toedieningsvorm. Het werkzame molecuul (API) is ongewijzigd. Dit betekent dus geen nieuw molecuul en geen nieuwe werkzame stof.
Deze vraag is begrijpelijk. De apotheekbereiding van lidocaïne met HP-β-cyclodextrine is (nog) niet vergoed door zorgverzekeraars, waardoor patiënten en artsen zoeken naar goedkopere alternatieven.
Standaard lidocaïne-infuusvloeistof is hier echter niet geschikt voor.
Deze vorm van lidocaïne wordt in de pijngeneeskunde uitsluitend in het ziekenhuis toegediend, onder continue medische bewaking. Toediening via een infuus of injectie (intraveneus of subcutaan) kan namelijk leiden tot te hoge lidocaïne-bloedspiegels, met risico op ernstige bijwerkingen. Daarom vindt deze behandeling alleen plaats in een klinische setting.
Voor vrijwel alle long-COVID-patiënten is het bovendien te belastend om herhaaldelijk naar het ziekenhuis te komen. Om veilige thuisbehandeling mogelijk te maken, is daarom een aangepaste samenstelling ontwikkeld, waarbij aan lidocaïne de hulpstof hydroxypropyl-β-cyclodextrine (HP-β-CD) is toegevoegd.
Met deze samenstelling wordt beoogd dat lidocaïne na toediening onder de huid bij voorkeur via het lymfestelsel wordt opgenomen en minder in het bloed om patienten in staat te stellen deze thuis op een veilige manier zelf te injecteren. Daarnaast maakt HP-β-CD de injecties minder pijnlijk en kan de werkzame dosis in een kleiner injectievolumeworden toegediend, wat het risico op opname in het bloed verder verkleint.
De veiligheid, bijwerkingen en resultaten van deze aangepaste lidocaïnebehandeling zijn onderzocht bij 103 patiënten met long COVID, die intensief en dagelijks werden gemonitord. Deze gegevens zijn recent wetenschappelijk gepubliceerd.
Het thuis injecteren van standaard lidocaïne-infuusvloeistof is daarentegen niet onderzocht en wordt om veiligheidsredenen nadrukkelijk afgeraden. Huisartsen en medisch specialisten wordt daarom geadviseerd lidocaïne-infuusvloeistof uitsluitend binnen het ziekenhuis toe te passen.
Er is wel degelijk follow-up na het stoppen of afbouwen van de behandeling. De gepubliceerde resultaten lopen tot april 2025; sindsdien gaan we door met het volgen van deze patiënten. We zijn momenteel een vervolg publicatie aan het voorbereiden met gegevens tot 66 weken. De voorlopige analyses laten zien dat de positieve effecten op zowel lichamelijke als mentale gezondheid in veel gevallen stabiel blijven of zelfs verder toenemen en dat een aanzienlijk deel van de patiënten de medicatie heeft kunnen afbouwen of volledig stoppen zonder terugval naar het oude klachtenniveau.
Tegelijkertijd vinden we het, juist vanwege de impact van deze bevindingen, belangrijk om de resultaten te bevestigen en te verfijnen in een formele, placebogecontroleerde Randomized Controlled Trial. Zo’n RCT wordt nu voorbereid.
Dat is een belangrijk misverstand. Veel mensen herstellen in de eerste maanden na een COVID-19-infectie, maar een aanzienlijk deel houdt langdurig klachten. Grote onderzoeken laten zien dat ongeveer 10–20% van de mensen na 12 maanden nog duidelijke klachten heeft die het dagelijks functioneren beïnvloeden. Als klachten langer dan een jaar bestaan, zien we dat spontaan herstel minder vaak voorkomt. Voor deze groep is long COVID geen korte nasleep, maar in veel gevallen een ernstige, invaliderende, chronische aandoening. Onze patiënten waren gemiddeld 2.5 jaar ernstig ziek zonder tekenen van verbetering met of zonder therapie.
Een ander misverstand is dat long COVID vooral zou voorkomen bij mensen die tijdens de corona crisis zeer ernstig ziek zijn geweest en/of op de intensive care hebben gelegen. De overgrote meerderheid van de ernstige long COVID-patiënten die wij hebben behandeld, ontwikkelde de ziekte enkele weken na een ‘gewone’ COVID-19-infectie, waarvan zij dachten bijna hersteld te zijn.
De studie in eClinicalMedicine is géén gewone observationele studie, maar een “interrupted time series” (ITS) studie, een methode die juist wordt gebruikt als alternatief voor wanneer een RCT (nog) niet haalbaar is. In deze opzet dienen patiënten in feite als hun eigen controlegroep.
Concreet betekent dit dat bij 103 post-COVID-patiënten eerst een pre-behandelingsperiode van gemiddeld 4 weken is gemeten, waarin zij dagelijks hun symptoom scores en tweewekelijks de SF-12 kwaliteits-van-leven vragenlijst invulden. Daarna zetten zij diezelfde metingen voort tijdens 36 weken behandeling met subcutane lidocaïne–HP-β-CD. Hierdoor ontstond een zeer gedetailleerd tijdsverloop van klachten voor en tijdens de behandeling, waarop analyses (linear mixed models) zijn toegepast.
Volgens prof. Jos Twisk, expert in longitudinale data-analyse en mede-auteur van de studie, benadert de statistische bewijskracht van deze ITS-opzet die van een RCT, doordat er zo veel herhaalde metingen zijn en iedere patiënt als eigen controle dient.
Voor deze studie is gebruikgemaakt van een interrupted time series-design. Dat betekent dat de scores van dezelfde groep patiënten op meerdere momenten zijn gemeten: vóór de start van de behandeling en gedurende de behandeling. Door deze metingen in de tijd met elkaar te vergelijken, kun je zien of er een verandering optreedt die samenhangt met het moment waarop de interventie wordt gestart. Alle patiënten zijn in deze analyse meegenomen, waardoor het gevonden effect een gemiddelde weerspiegeling is van de hele groep, inclusief de uitvallers. Binnen die groep zijn uiteraard mensen bij wie het duidelijk beter ging, maar ook mensen bij wie de verbetering minder groot of afwezig was. Ook waren er enkele patiënten die verslechtering rapporteerden.
Voor de uitkomstmaten is onder andere gebruikgemaakt van de Mental Component Summary (MCS) en Physical Component Summary (PCS) scores van een gevalideerde vragenlijst (de SF-12). De MCS meet mentale gezondheid, de PCS meet fysieke gezondheid. In de algemene bevolking liggen deze scores gemiddeld rond de 50 punten, met een standaarddeviatie van ongeveer 10 punten. Hogere scores duiden op een betere gezondheid.
De kleinste verandering in score die merkbaar is voor patiënten wordt ook wel de Minimal Clinically Important Difference (MCID) genoemd. Voor Long COVID bestaat op dit moment nog geen vastgestelde MCID. Bij andere chronische aandoeningen ligt de MCID voor de MCS doorgaans in de orde van 3–5 punten. Dit geeft een indicatie van wat als klinisch relevant kan worden beschouwd, al moet dit voor Long COVID nog specifiek worden vastgesteld.
De gevonden verbetering van 4.13 op de PCS score en 7 punten op de MCS score bij 36 weken is groter dan wat doorgaans als klinisch relevant wordt beschouwd, wat erop wijst dat de behandeling voor veel patiënten een betekenisvolle verbetering heeft opgeleverd.
Als je alleen naar de cijfers +7 (MCS) en +4 (PCS) kijkt, lijkt dat niet spectaculair. Maar die getallen zijn een samenvatting van het verloop van alle 103 patiënten samen. In die groep zitten mensen die duidelijk opknappen, mensen die beperkt verbeteren en mensen die weinig of niet reageren. We gebruiken een intention-to-treat analyse in combinatie met een lineair mixed model. Eenvoudig gezegd: het model gebruikt alle beschikbare metingen van alle patiënten over de tijd en trekt daar een gemiddelde lijn doorheen. Ook patiënten die eerder stoppen of een meting missen, blijven gewoon meetellen. Dat is eerlijker en realistischer dan alleen de mensen mee te nemen die de behandeling volledig afmaken, maar het zorgt er wél voor dat het groepsgemiddelde lager uitvalt dan de verbetering die een deel van de patiënten laten zien.
Het gemiddelde van +7 (MCS) en +4 (PCS) betekent dus niet dat iedereen maar een klein beetje vooruit gaat. In de verdeling zie je dat een flinke groep patiënten grote stappen maakt in mentale en/of lichamelijke gezondheid, een deel gematigd verbetert en een kleinere groep weinig tot niet verandert. Juist die grotere groep die duidelijk opknapt, is een belangrijke reden om de behandeling voort te zetten. Daarnaast kijken we naar wat in de geneeskunde een klinisch relevante verandering wordt genoemd (MCID). Voor long COVID is nog geen officiële grens vastgesteld, maar bij andere chronische aandoeningen wordt een verbetering van ongeveer 3–5 punten op dit soort schalen al gezien als merkbaar en relevant. De verbeteringen die wij zien (+7 en +4 gemiddeld over de hele groep) liggen in of boven die range. Dit sluit ook aan bij wat patiënten zelf aangeven: 78% rapporteert een duidelijke verbetering van kwaliteit van leven. Gezien het feit dat het gaat om een chronische ziekte met langdurige ernstige klachten zijn dit betekenisvolle resultaten. Daarom concluderen we dat er bij een groot deel van de patiënten een duidelijk en relevant behandeleffect is, en vormt dit een stevige reden om de behandeling én het verdere onderzoek voort te zetten.
Naast de vragenlijsten die afgenomen zijn via de app, is ook een Global Perceived Effect vragenlijst (GPE) afgenomen. Patiënten vulden deze GPE vragenlijst bij ons in de kliniek tijdens de terugkomdagen in. Deze vonden elke zeven weken plaats.
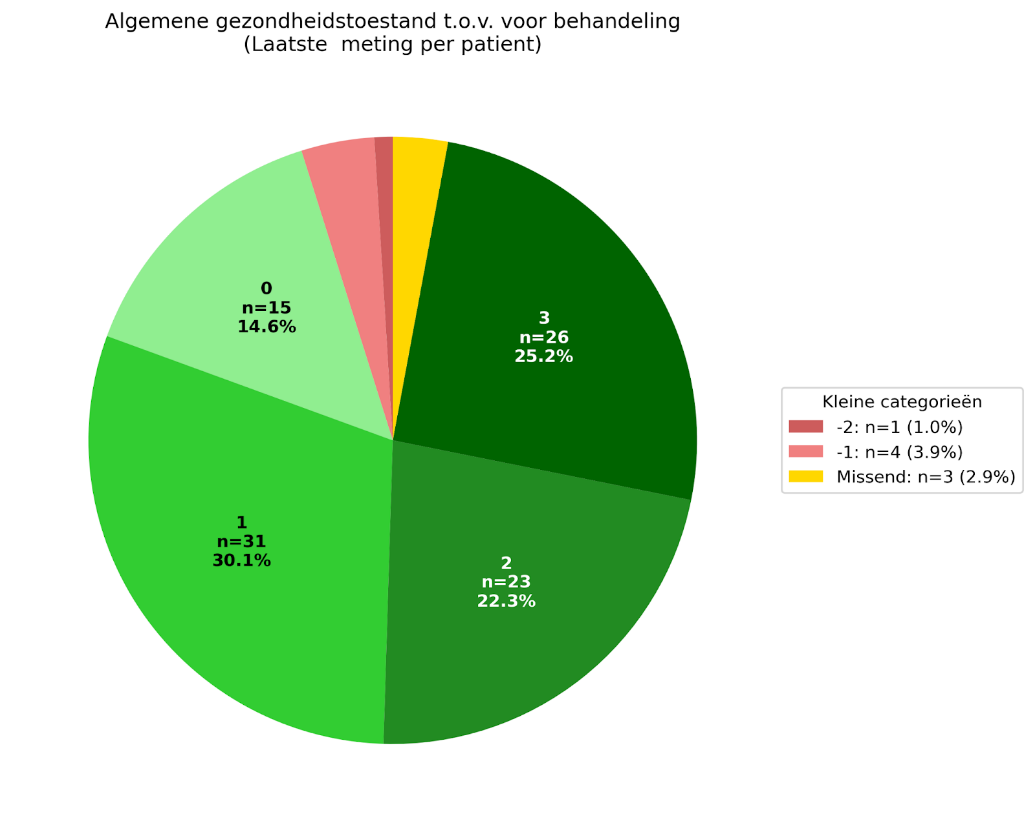
Het percentage van 78% is gebaseerd op de positieve scores ( 1. Iets beter, 2. Beter en 3. Veel beter) op de vraag “Hoe beoordeelt u uw algemene gezondheidstoestand in vergelijking met voordat u met de behandeling begon?”. Dit percentage is berekend over de volledige onderzoeksgroep van 103 patiënten bij de 36-weken meting. Deze aanpak sluit aan bij de gekozen onderzoeksopzet, waarbij in alle analyses steeds de volledige groep patiënten over de gehele meetperiode is meegenomen. Hierin zijn de laatst ingevulde GPE-scores van alle patiënten meegenomen, inclusief die van de vroegtijdig gestopte patiënten. Er waren 30 patiënten vroegtijdig gestopt. Dit betekent niet per definitie dat deze patiënten geen baat hebben gehad bij de behandeling. De redenen voor vroegtijdig stoppen waren uiteenlopend. Een deel van de vroegtijdige stoppers had een positieve GPE-score gegeven. In totaal had 80 van de 103 patiënten een positieve GPE-score. 20 patiënten vielen in de categorie met negatieve of neutrale GPE-score, en van 3 patiënten ontbraken de GPE-data. De positieve GPE-score, 80 van de 103 patiënten, komt overeen met 78% van de totale onderzoeksgroep die in het artikel is opgenomen.
Voor de beantwoording van deze vraag is het onderscheid tussen incidenten / events en bijwerkingen (adverse events) belangrijk.
Een incident is een ongewenste gebeurtenis tijdens de behandeling of in het zorgproces (een klacht die optreedt, een injectie die onbedoeld in een bloedvat terecht komt, een blauwe plek na het prikken etc.). Pas later wordt beoordeeld of een incident een bijwerking is: Adverse Event (AE): bijwerking ongeacht of er een link is met het medicament, een Adverse Drug Reaction (ADR): bijwerking waarschijnlijk of bevestigd veroorzaakt door het medicament of een Serious Adverse Event (SAE)/Serious Adverse Drug Reaction (SADR), een ernstige bijwerking met een ernstig gevolg, zoals overlijden, een levensbedreigende situatie, (verlengde) ziekenhuisopname of blijvende schade (ICH-richtlijnen voor Good Clinical Practice).
In totaal zijn er 64,281 injecties voorgeschreven in de periode tot 36 weken na de start van de behandeling. In deze periode zijn er 73 incident meldingen binnengekomen van (gedeeltelijke) intravasculaire injectie (in de bloedbaan), afkomstig van 34 patiënten in totaal. Een injectie in de bloedbaan kan leiden tot klachten zoals: duizeligheid, tintelingen rond de lippen, oorsuizen, hoofdpijn, en (neiging tot) flauwvallen. Deze klachten waren kortdurend en reversibel. Enkele patiënten hebben hierna aangegeven PEM klachten vergelijkbaar met een te grote inspanning te hebben ervaren. Bij vier incidenten heeft dit tot een 112-melding geleid, waarvan één tot een eerstehulpbezoek per ambulance. Na evaluatie door een eerstehulparts kon de patiënt weer naar huis. Op basis van de eerder genoemde ICH-richtlijnen is geen van deze incidenten als een SAE geclassificeerd. Het incident waarbij de patiënt op de eerste hulp is beoordeeld, is gemeld bij de Inspectie Gezondheidszorg en Jeugd (IGJ). Na het aanpassen van de prikinstructies (o.a. injecteren over 120 seconden en roteren van injectieplaats) nam het aantal gerapporteerde intravasculaire injecties af met 83%
De huidreacties die bij de dagelijkse subcutane injecties kunnen optreden, worden in het artikel als “milde bijwerking” geclassificeerd omdat ze geen blijvende schade veroorzaken. In klinisch onderzoek worden bijwerkingen ingedeeld naar ernst: mild, matig, of ernstig (severity grading). Huidreacties zoals roodheid, zwelling, bloeduitstortingen of verhardingen vallen in de categorie mild adverse events.
Dat betekent niet dat deze klachten voor patiënten niet vervelend kunnen zijn. Echter, veel patiënten vonden de huidreacties ten gevolge van de dagelijkse injecties niet hinderlijk in verhouding tot de ervaren verbetering van hun klachten. De huidproblemen verdwijnen doorgaans binnen enkele weken tot maanden na het afbouwen/stoppen van de injecties.
Huidreacties zijn te verwachten bij frequente subcutane injecties, zoals ook bekend is bij bijvoorbeeld insuline- of antistollingsbehandelingen. Wel vragen deze reacties om aandacht. In de loop van de tijd zijn verschillende strategieën ingezet om de huid zo goed mogelijk te ondersteunen en problemen te beperken, zoals koelen, masseren, lymfedrainage, het gebruik van raster pleisters, en het regelmatig wisselen van injectieplaatsen.
In de studie beschrijven we de resultaten tot en met 36 weken na start van de behandeling, maar in de praktijk varieert de behandelduur per patiënt. Patiënten worden doorgaans meerdere maanden behandeld; de behandeling wordt voortgezet totdat iemand stabiel hersteld is tot ongeveer 80% van het functioneren van vóór het ontstaan van de ziekte. Op dat moment wordt in samenspraak tussen patiënt en behandelend arts gestart met afbouwen en, waar mogelijk, stoppen.
De behandeling bestaat uit subcutane (onderhuidse) injecties met lidocaïne-HP-β-CD, die patiënten thuis zelf toedienen volgens een vast schema. Tijdens de behandeling worden zij intensief gemonitord: patiënten rapporteren via een webapplicatie dagelijks de ernst van hun klachten, vullen op vaste momenten uitgebreidere vragenlijsten in, en komen ongeveer elke zes weken voor een klinische controle. Zo kunnen het beloop van de klachten, het moment van afbouwen en de veiligheid van de behandeling nauwkeurig worden gevolgd.
Voor Long Covid wordt geschat dat wereldwijd circa 450 miljoen mensen kampen met chronische, niet-spontaan verbeterende klachten. In Nederland gaat het naar schatting om 350.000–400.000 mensen (ongeveer 2–2,5% van de bevolking) met langdurige klachten, van wie rond de 100.000 ernstig ziek zijn.
Veel van deze ernstig zieke patiënten raken (deels) uit beeld, omdat er nog geen betrouwbare diagnostische test beschikbaar is. Medisch specialisten zoals neurologen, cardiologen en longartsen vinden in bloedonderzoek of op beeldvorming meestal weinig afwijkingen die de ernst van de klachten kunnen verklaren. Daardoor is de aandoening lange tijd óf benaderd als een lastig te duiden multisysteemziekte met verschillende mogelijke onderliggende mechanismen, óf – ten onrechte – vooral als psychosomatisch geïnterpreteerd, met grote medische, sociale en financiële gevolgen voor patiënten.
Het groeiende inzicht dat long covid waarschijnlijk een belangrijke immunologische component heeft en in elk geval bij een deel van de patiënten behandelbaar lijkt, luidt naar verwachting een nieuwe fase in, zowel voor patiënten als voor zorgverleners. De hier beschreven therapie is specifiek gericht op mensen met ernstige, invaliderende klachten; dat is een zeer grote groep, in Nederland en wereldwijd, voor wie nu nog nauwelijks effectieve behandelopties beschikbaar zijn.
Excellent Care Clinics (ECC) is al vier tot vijf jaar bezig om een behandeling voor long COVID stap voor stap te verbeteren. In deze periode is er veel tijd, energie en geld geïnvesteerd, zonder steun van de overheid (subsidie) of een groot farmaceutisch bedrijf. Op basis van deze ontwikkeling is besloten om de vindingen te patenteren. Het gaat daarbij niet om lidocaïne zelf, dat is een oud en goedkoop geneesmiddel waarvan de patenten al lang zijn verlopen, maar om de nieuwe samenstelling en toedieningswijze die specifiek is gericht op de lymfeklieren/het immuunsysteem.
Het doel van deze patenten is om deze, zodra de nieuwe werking met goed wetenschappelijk onderzoek voldoende is aangetoond, over te dragen aan een aan een internationaal farmaceutisch bedrijf. Zo’n partij kan de enorme kosten dragen die nodig zijn voor internationale registratie, het vervolgens op grote schaal produceren, tegen lage kosten per patiënt, en er daarmee voor zorgen dat de behandeling uiteindelijk voor zoveel mogelijk mensen, ook buiten Nederland, beschikbaar komt. Zonder patentbescherming zal geen enkele partij bereid zijn de ontwikkel- en registratiekosten op zich te nemen. ECC is een medische onderneming die volgens principes van good governance de plicht heeft om het zorgbedrijf economisch gezond te laten functioneren. Dat is nodig om continuïteit van zorg te kunnen garanderen, zorgpersoneel te kunnen betalen en te kunnen blijven investeren in nieuwe apparatuur en verdere innovatie. In dat licht is het wenselijk dat de patenten er ook aan bijdragen dat het geïnvesteerde geld op termijn kan worden terugverdiend. Het gaat daarbij niet om winstmaximalisatie, maar om een voorwaarde om behandelingen verder te ontwikkelen, betaalbaar en grootschalig beschikbaar te maken en de continuïteit van goede zorg te waarborgen.
In onderzoek kun je twee soorten uitkomsten meten: objectieve metingen en subjectieve metingen. Objectieve metingen zijn bijvoorbeeld bloedtesten, scans, of andere biomarkers die los staan van hoe iemand zich voelt. Subjectieve metingen zijn vragenlijsten waarin patiënten zelf aangeven hoe het gaat met hun klachten, functioneren, en kwaliteit van leven.
Voor long COVID zijn er op dit moment geen betrouwbare objectieve metingen beschikbaar. Er bestaat nog geen bloedtest, scan, of andere biomarker die duidelijk kan laten zien of iemand long COVID heeft en of een behandeling werkt. Wereldwijd wordt hiernaar gezocht, maar deze metingen zijn nog niet voldoende ontwikkeld of bewezen.
Long COVID wordt door internationale experts gedefinieerd als een chronische klachten stoornis na SARS-CoV-2 infectie, met een breed scala aan symptomen (vermoeidheid, cognitieve problemen, inspanningsintolerantie, pijn, etc.) die sterk bepalen wat iemand nog kan in het dagelijks leven. Die klachten zijn per definitie wat de patiënt voelt en ervaart. Daarom zijn vragenlijsten over: lichamelijk functioneren (PCS, lichamelijke subschaal SF-12), mentaal functioneren (MCS, mentale subschaal SF-12), en globale verbetering (GPE / “hoe gaat het nu t.o.v. eerder?”), op dit moment de meest directe en klinisch relevante manier om te meten of iemand daadwerkelijk vooruitgaat.
Daarom zijn subjectieve uitkomsten nu de norm in long-COVID-onderzoek. Grote internationale onderzoeken werken hiermee, en ook de European Medicines Agency (EMA) geeft aan dat deze uitkomsten op dit moment een acceptabele en geschikte manier zijn om effect van behandeling te meten bij long COVID.
We sluiten aan bij wat internationaal als beste beschikbare methode geldt: symptoom scores en kwaliteit-van-leven-vragenlijsten als primaire uitkomst. Die zijn ook precies wat in recente grote long-COVID-studies wordt gebruikt. In vervolgonderzoek (zoals de geplande RCT) willen we naast deze subjectieve uitkomsten wel biomarkers meten, zodat we in de toekomst hopelijk ook meer objectieve uitkomstmaten kunnen inzetten.
Kortom: omdat er nog geen objectieve metingen voor long COVID bestaan, zijn vragenlijsten en patiënt gerapporteerde uitkomsten nu wereldwijd de standaard en de best beschikbare methode om te bepalen of iemand daadwerkelijk vooruitgaat.
Nee. Het betrof reguliere zorg: patiënten werden behandeld volgens de gebruikelijke klinische praktijk binnen onze kliniek. Pas nadat de eerste behandelresultaten beschikbaar waren, zijn deze bestaande gegevens retrospectief geanalyseerd door onderzoekers van de Vrije Universiteit en Amsterdam UMC. Omdat er geen extra handelingen, geen randomisatie en geen onderzoeksinterventie plaatsvonden, viel dit onder observationeel real-world onderzoek en was er geen WMO*-verklaring nodig.
*WMO (Wet medisch-wetenschappelijk onderzoek met mensen): Nederlandse wet die bepaalt wanneer voorafgaande toetsing door een medisch-ethische commissie verplicht is bij onderzoek waarbij proefpersonen extra handelingen, metingen of gedragsregels krijgen die niet tot de reguliere behandeling behoren.